|
徐衎1,李洲鹏1,刘宾虹2,秦海英1
(1.浙江大学化学工程与生物工程学系;2.材料科学与工程学系,浙江杭州310012)
摘要:综述了近几年来关于最具商业前景的直接二甲醚燃料电池的研究成果,文中主要探讨了新型阳极催化剂的开发,膜电极结构对电池性能的优化以及操作条件对电池性能的影响。建议在深入对催化剂、电池结构和操作条件的研究基础上,采用碱性电解质饱和二甲醚为燃料和双氧水替代氧气为氧化剂等方法进一步提高电池性能。
0前言
近几年来,质子交换膜燃料电池(PEMFC)被看作移动式和便携式电源领域最有前景的技术之一[1-3],然而其商品化还面临氢的生产和储运问题。人们尝试寻找其它的替代燃料以克服PEMFC的技术障碍。
直接甲醇燃料电池(DMFC)的催化剂活性低且极易中毒,甲醇在阴极和阳极之间渗透会造成电池性能的严重损失。对直接乙醇燃料电池[4]的研究表明,乙醇的分子结构中存在C-C键,难以彻底氧化成CO2;有人尝试使用二甲氧基甲烷(DMM)和三甲氧基甲烷(TMM)[5,6]作为燃料,但是两种有机物氧化后有甲醇生成,依旧存在燃料渗透问题,并且这两种有机物制备成本较高。因此人们提出了以二甲醚作为燃料的直接二甲醚燃料电池(DDFC)。二甲醚(DME)是一种无毒,可溶于水的有机物,常温常压下以气体形式存在,在0.6MPa的压力下可被液化,便于储存与运输。DDFC理论比能量密度较高(8.2kWh·kg-1),理论电动势为1.194V,与DMFC(1.183V)以及PEMFC(1.229V)相当,且DDFC的理论热力学效率较高(95%)。
二甲醚来源广泛,可从石油、天然气、煤、生物质等多种原料制得,结合我国煤炭资源的优势,规模化生产的成本较低,因此,将二甲醚能源与PEMFC技术相结合而产生的DDFC很有希望成为大规模商业化应用的便携和移动式电源,如电动汽车,电子产品和军用设备等。
1直接二甲醚燃料电池的研究进展
1.1二甲醚电催化氧化机理研究进展
国内外学者针对二甲醚的在铂催化剂上的电催化氧化机理进行了广泛且深入的研究,试图从根本上提高其电化学反应活性。由于在二甲醚电氧化副产物中发现一定量的甲醇,Muller等[7]提出二甲醚分子脱氢吸附在Pt上后,水解产生Pt-COH和CHOH分子。而Tasutasumi等[8]在基于对阳极氧化产物的研究基础上,提出不同的反应机理。他们的研究结果显示,在80℃和常压下,阳极侧仅发现甲酸,并且甲酸的含量随着电流密度的增加而提高,因此推断二甲醚分子的吸附需要两个Pt活性位,先形成Pt2-CH-O-CH-Pt2,之后水解产生Pt-COH,最终氧化为CO2。
Mizutani等报道了二甲醚在Pt/C催化剂上氧化的数据[9]。阳极反应产物的分析表明,二甲醚在高温下大部分被氧化为CO2,主要副产物为甲醇和甲酸甲酯。甲醇可能是二甲醚的水解产物,而甲酸甲酯的生成速率是由电流密度和温度共同决定的,因而可能是电化学氧化反应的产物,在较高的温度下,二甲醚更加倾向于生成CO2而不是HCOOCH3。
关于二甲醚在片状铂电极上的电化学氧化研究,Kerangueven等[10]利用原位红外反射光谱技术检测到Pt电极上存在直线型COL(2050cm-1)吸附物和桥式COB(1950cm-1)吸附物以及HCOOads(1702cm-1)吸附物。作者认为低电位下(≤0.55Vvs.RHE)二甲醚分子在Pt上吸附产生Pt-CHO或Pt-CO,随后在非活性水参与下反应生成CHOOH或CO2。高电位(>0.55Vvs.RHE)下水分子被活化并在Pt上形成含氧活性物质Pt-OH。最近,Liu等[11]利用电化学工作站和原位傅立叶红外转换全反射转换光谱(ATR-FTIR),发现在0.1~0.45V的电压范围内,铂电极表面吸附产物覆盖率达到90%。除了CO,电极表面主要的中间吸附产物包括-COOH,-CHO,-HCOO-和-OCH3。
2.2直接二甲醚燃料电池阳极催化剂的研究
在直接甲醇燃料电池阳极催化剂的研究中,Pt-M(M包含Ru,Sn,W,Mo)[12]合金不但具更高的催化活性,而且对于CO有更强的抗毒化能力。因而对于二甲醚电氧化催化剂的开发按照同样的原则,即基于Pt金属的二元合金。
Liu等[13]将一系列不同Pt∶M比例的碳载体催化剂(PtRu/C,Pt3Sn/C,PtW/C,Pt3Mo/C,PtCo/C,PtNi/C,Pt2Cr/C)与Pt催化剂进行了对比。在0.55V以下,PtRu/C和Pt3Sn/C催化剂的活性明显的高于Pt/C和其他PtM/C催化剂。然而当电压高于0.6V,氧化过程中生成的可毒化吸附物在粗糙的铂电极表面更有效的被氧化为CO2,Pt/C却比PtRu/C对二甲醚的电化学氧化活性更高。
Coutanceau与其合作者对不同合金比例的PtRu/C和PtSn/C催化剂进行了研究[10]。发现在Pt金属中加入Ru和Sn,并没有影响开路电压(0.8V)。
Müller将这种现象归之为二甲醚的渗透不影响阴极的极化[7]。在阴极电势下,二甲醚在阴极催化剂上不会发生吸附并氧化。无论是否形成合金,恒定的开路电压表明,二甲醚在Pt电极上的吸附电位与Ru或Sn非常接近。Ru和Sn并没有表现出和协同催化作用,这与甲醇在PtRu/C上[14]和乙醇在PtSn/C上[15]的吸附是完全不同的。但是,使用Pt0.5Ru0.5,Pt0.8Ru0.2,Pt0.9Sn0.1催化剂的燃料电池在电流密度分别低于20,250和180mA·cm-2时,性能都高于使用Pt催化剂的电池。这是因为在低电压下,Ru和Sn比Pt更能够活化水分子,生成更多的氧原子帮助完全氧化二甲醚的电化学氧化到CO2或者HCOOH。
2.3直接二甲醚燃料电池膜电极的结构对电池性能的影响
影响电池性能的一个关键因素就是膜电极的制备过程,还需要考虑到阴阳两极的实际反应过程,燃料的注入,水管理等一系列因素。最近,很多学者报告了膜电极结构对电池性能的影响[9,16,17]。
Mench等研究了膜的厚度对于膜电极性能的影响。发现阳极过于干燥,使用较厚的Nafion膜时(厚度为178μm)会导致性能的急剧下降,此外,较薄的Nafion112(厚度为51μm)使得二甲醚和其氧化过程中间产物的严重渗透而无法使用。Nafion115(厚度为127μm)有效促进了阴极的水份渗透到阳极。
Cai等研究了气体扩散层憎水性对于性能的影响[18]。作者分别比较了憎水,一半面积憎水以及全部亲水的扩散层组装成的膜电极的电池性能。在低电流密度时,三者差异不大,而电流密度不断增大,一半面积憎水的膜电极表现出优越的性能。阻抗分析表明,修饰后的膜电极有效降低传质阻力。
2.4直接二甲醚燃料电池操作条件的研究
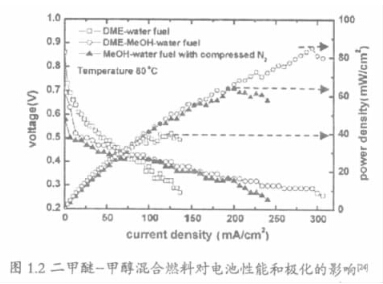
改变工作条件可以有效优化直接二甲醚燃料电池性能。Cho和合作者对此进行了一系列的研究[13,19,20],在常压下,将饱和二甲醚的水溶液作为燃料注入电池,电池性能明显优于对二甲醚充分加湿后以气体方式注入的方式。此外,他们还研究了压力对电池性能的影响。当操作压力高于300KPa以后,电池性能显著优于常压操作条件。Yoo等最近研究了以二甲醚和甲醇混合燃料的电池性能[20]。如图1.2所示,使用混合燃料的电池最大输出功率达到约85mW·cm-2,预计其中二甲醚贡献了24%的性能,他们认为将二甲醚溶解于水或其他燃料形成混合燃料,可以在较低的温度下强化二甲醚燃料电池的性能,降低DDFC的启动温度。
3直接二甲醚燃料电池新的发展方向
关于DDFC研究的核心目标是有效提高电池性能,这是其商业化的关键所在。然而至今为止,研究人员始终无法突破性的提高电池性能,DDFC的进一步发展需要对DDFC做更加全面的研究工作。参考其他质子交换膜燃料电池的技术研发,笔者对DDFC的发展建议了一些新的方向:
(1)碱性介质有利于小分子有机物的氧化,运用碱性电解液饱和二甲醚作为燃料,不仅有利于二甲醚的电化学氧化,而且相比于水溶液,可以显著降低阳极离子传导阻力。同时碱性条件下,氧气在阴极的电化学还原反应速率更快。因此,使用碱性溶液饱和二甲醚将很有希望提高DDFC的性能和稳定性。
(2)使用双氧水作为阴极还原剂可以显著提高阴极电位,Luo等[21]将双氧水应用于直接硼氢化钠燃料电池(DBFC),替代氧气作为氧化剂,在65℃、常压下,得到电池最大输出功率1.5W·cm-2,大幅度提高了DBFC的性能。因此,可以尝试研究直接二甲醚/双氧水燃料电池,以期获得电池性能的飞跃。
4结论
综上所述,笔者总结了国内外学者从阳极催化剂、膜电极结构和电池操作条件三个方面在直接二甲醚燃料电池(DDFC)领域取得的主要研究成果。然而相比于直接甲醇燃料电池[22]、直接硼氢化钠燃料电池[23,24]而言,因而有待更深入的研究。在此基础上,笔者建议研究碱性电解质溶解二甲醚为燃料和双氧水替代氧气为还原剂的发展方向。随着对DDFC的深入研究和发展,必将取得更大的突破。
参考文献:
[1]Zhou Y K,et al.Improving PEM fuel cell catalyst activity and durability using nitrogen-doped carbon supports:observations from model Pt/HOPG systems[J].Journal of Materials Chemistry,2009,19(42):7830-7838.
[2]Tongamp W,et al.Generation of hydrogen from polyvinyl chloride by milling and heating with CaO and Ni(OH) 2[J].Journal of Hazardous Materials,2009,167(1-3):1002-1006.
[3]Maheshwari P H,Mathur R B.Improved performance of PEM fuel cell using carbon paper electrode prepared with CNT coated carbon fibers[J].Electrochimica Acta,2009,54(28):7476-7482.
[4]James D D,et al.Online analysis of products from a direct ethanol fuel cell[J].Electrochemistry Communications,2009,11(10):1877-1880.
[5]Narayanan S R,et al.Direct electro-oxidation of dimethoxymethane,trimethoxymethane,and trioxane and their application in fuel cells[J].Journal of the Electrochemical Society,1997,144(12):4195-4201.
[6]Wang J T,et al.A H-2/O-2 fuel cell using acid doped polybenzimidazole as polymer electrolyte[J].Electrochimica Acta,1996,41(2):193-197.
[7]Muller J T,et al.Electro-oxidation of dimethyl ether in a polymer-electrolyte-membrane fuel cell[J].Journal of the Electrochemical Society,2000,147(11):4058-4060.
[8]Tsutsumi Y,et al.Direct type polymer electrolyte fuel cells using methoxy fuel[J].Electrochemistry,2002,70(12):984-987.
[9]Mizutani I,et al.Anode reaction mechanism and crossover in direct dimethyl ether fuel cell[J].Journal of Power Sources,2006.156(2):183-189.
[10]Coutanceau C,et al.Methoxy methane (dimethyl ether) as an alternative fuel for direct fuel cells[J].Journal of Power Sources,2006,157(1):318-24.
[11]Liu Y,et al.Electrochemical and ATR-FTIR study of dimethyl ether and methanol electro-oxidation on sputtered Pt electrode[J].Electrochimica Acta,2007,52(19):5781-5788.
[12]Wang J H,Nakajima,Kita H.Metal-electrodes bonded on solid polymer electrolyte membrane (spe).6.methanol oxidation on molybdenum modified pt-spe electrode[J].Electrochimica Acta,1990,35(2):323-328.
[13]Liu Y,et al.Electro-oxidation of dimethyl ether on Pt/C and PtMe/C catalysts in sulfuric acid[J].Electrochimica Acta,2006,51(28):6503-6509.
[14]Waszczuk P,et al.Adsorption of CO poison on fuel cell nanoparticle electrodes from methanol solutions:a radioactive labeling study[J].Journal of Electroanalytical Chemistry,2001,511(1-2):55-64.
[15]Vigier F,et al.On the mechanism of ethanol electro-oxidation on Pt and PtSn catalysts:electrochemical and in situ IR reflectance spectroscopy studies[J].Journal of Electroanalytical Chemistry,2004,563(1):81-89.
[16]Mench M M,Chance H M,Wang C Y.Direct dimethyl ether polymer electrolyte fuel cells for portable applications[J].Journal of the Electrochemical Society,2004,151(1):A144-A150.
[17]Eguchi M,et al.Electrochemical characteristics of direct dimethyl ether fuel cells[J].Solid State Ionics,Diffusion & Reactions,2006,177(19-25):2175-8.
[18]Cai K D,et al.Investigation of a novel MEA for direct dimethyl ether fuel cell[J].Electrochemistry Communications,2008,10(2):238-241.
[19]Yu R H,Choi H G,Cho S M.Performance of direct dimethyl ether fuel cells at low temperature[J].Electrochemistry Communications,2005,7(12):1385-1388.
[20]Yoo J H,et al.Fuel cells using dimethyl ether[J].Journal of Power Sources,2006,163(1):103-106.
[21]Luo N,et al.NaBH4/H2O2 fuel cells for air independent power systems[J].Journal of Power Sources,2008,185(2):685-690.
[22]Chang Y M,Hsieh Y C,Wu R W.Improved electrochemical performances by carbon nanocapsules as an electrocatalyst support for direct methanol fuel cells[J].Diamond and Related Materials,2009,18(2-3):501-504.
[23]Li Z P,et al.Depression of hydrogen evolution during operation of a direct borohydride fuel cell[J].Journal of Power Sources,2006,163(1):555-559.
[24]Liu B H,Li Z P,Suda S.Electrocatalysts for the anodic oxidation of borohydrides[J].Electrochimica Acta,2004,49(19):3097-3105. |

